Die Erstbeschreibung erfolgte vor mehr als 100 Jahren (Howell, W. H. (1890). The life-history of the formed elements of the blood, especially the red blood corpuscles. Journal of Morphology, 4:57–116. Jolly, J. (1908) Recherches sur la formation des globules rouges des mammifères, 58. Paris: Comptesrendus de la Société de Biologie, 528–531).
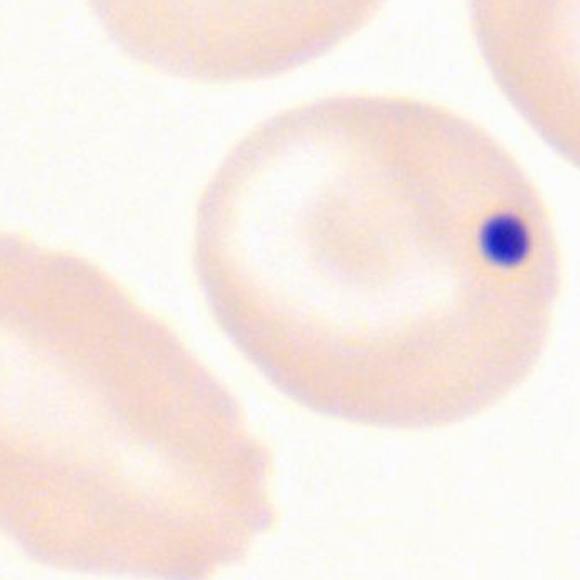
Abb. 1: Papp, BB, Ery mit Howell-Jolly-K. © UK Aachen
Entstehungsmechanismus
HJ-K entstehen während der Ausstoßung des Erythroblastenkerns dann, wenn sich kleinere Kernfragmente abgetrennt haben und nach der Entfernung des Hauptkerns im Erythrozyten sozusagen als Geburtsfehler verbleiben. Der Kernrest wird durch die intensive Bewegung des Erythrozyten während der Zirkulation in der Blutbahn rund wie ein Stein im Meer. Das Vorhandensein von HJ-K im Blutausstrich ist immer pathologisch. Das HJ-K bleibt solange im Erythrozyten bis dieser das erste Mal in die Milz gelangt. Dort wird das HJ-K entfernt.
Milz und Howell-Jolly-Körperchen
Die Milz besteht aus der roten und weißen Pulpa. Während die weiße Pulpa lymphatischem Gewebe entspricht, besteht die rote Pulpa aus den Milzsinus. Das sind seenartige Räume, in die sich das Blut mit seinen korpuskulären Anteilen aus den offen endenden Ateriolen ergießt. Die Blutbestandteile werden nachfolgend in haarförmig dünnen Blutgefäßen, den Sinus, gesammelt und schließlich den Venen zugeführt.
Beim Übertritt der Erythrozyten aus dem Blutsee der roten Pulpa in die venösen Sinus, müssen sie sich durch schmale Spalten zwischen den die Sinus auskleidenden Endothelzellen hindurchquetschen (Abb. 2 und Abb. 3). Bei diesem Vorgang werden korpuskuläre Anteile herausgemangelt. Dementsprechend werden die HJ-K als Kernreste herausgedrückt. Bei fehlender Milz nach Splenektomie oder bei funktioneller Asplenie unterbleibt die Nachbesserung des Geburtsfehlers. Die Folge ist der Verbleib von HJ-K im Blutausstrich.
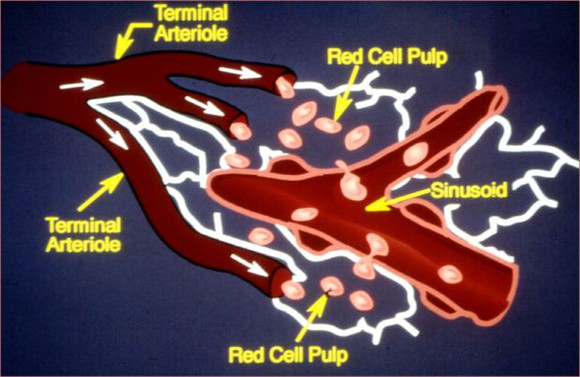
Abb. 2: Rote Pulpa der Milz. Die Erythrozyten zwängen sich durch die engen Endothelspalten und werden dadurch von korpuskulären Partikeln befreit. © aus R. Fuchs et al. Manual Hämatologie 2015, Nora-Verlag.
Abb. 3: Vergößerter Ausschnitt zu Abb. 2. Ery quetscht sich durch eine Lücke zwischen Endothelzellen.
Vorkommen von Howell-Jolly-Körperchen
HJ-K bei fehlender oder funktionsloser Milz
- Neugeborene und Frühgeborene als Zeichen der unreifen Milz (Hyposplenie)
- Zustand nach Splenektomie
- Funktionelle Asplenie z.B. bei Sichelzellkrankheit.
HJ-K bei vorhandener und funktionierender Milz
- Schwere Bildungsstörungen der Erythropoese
- Megaloblastäre Anämie
- Majorform der Thalassämie
- Myelodysplastisches Syndrom
- Erythroleukämie.
Differenzialdiagnosen
HJ-K müssen von anderen intraerythrozytären Einschlüssen abgegrenzt werden: Pappenheimer-Körperchen, die Eisenpartikeln entsprechen und ebenfalls nach Milzentfernung vorkommen, sind kleiner als HJ-K und liegen häufig in Gruppen (Abb. 4). Malaria Plasmodien zeigen eine siegelringförmige Gestalt. Schwierig kann die Abgrenzung zu Schmutzpartikeln sein. Beim Betätigen der Mikrometerschraube des Mikroskops zeigen Artefakte eine Lichtbrechung und leuchten auf, während HJ-K abblassen und verdämmern. Heinz’sche Innenkörperchen, die denaturiertem Hämoglobin entsprechen, stellen keine echte Differenzialdiagnose zu HJ-K dar, da man diese nur mittels Supravitalfärbung nachweisen kann.
Literatur
1. Bain J, Huhn D. Roche Grundkurs hämatologische Morphologie, Blackwell Wissenschafts-Verlag, Wien 1997: 65-66.
2. Fuchs R et al. Manual Hämatologie, Nora-Verlag, Stolberg 2015: Seiten 59; 206-208; 263.
3. Diggs LW, Sturm D, MS A Bell. The morphology of human blood cells. 7th ed., Abbott 2005: Seite 16-17
Der Autor:
Prof. Dr. med. Roland Fuchs
Uniklinik Aachen
Klinik für Hämatologie, Onkologie, Hämostaseologie
und Stammzelltransplantation
Die Autorin:
Reinhild Herwartz
Biomedizinische Fachanalytikerin Hämatologie
Uniklinik Aachen, Klinik für Hämatologie, Onkologie,
Hämostaseologie und Stammzelltransplantation
E-Mail: reinhild@herwartz.de
Entnommen aus MTA Dialog 12/2015
Dann nutzen Sie jetzt unser Probe-Abonnement mit 3 Ausgaben zum Kennenlernpreis von € 19,90.
Jetzt Abonnent werden

