Mit einer Fläche von etwa 2 m² stellt die Haut (gr. derma; lat. cutis) das größte Organ des menschlichen Körpers dar. Sie erhält circa ein Drittel der ganzen Blutversorgung im Organismus. In erster Linie erfüllt sie als Hüllorgan eine Schutzfunktion aus: Sie verhindert das Eindringen von Fremdkörpern und Mikroorganismen. Zudem verhindert sie den Verlust existenzieller endogener Stoffe wie Wasser und Elektrolyte und ist eine effiziente Barriere [2]. Sie schützt vor Wärmeverlust und dient der Aufnahme von Sinnesreizen. Das macht die Haut zu einem untypischen Resorptionsorgan.
Die Hautoberfläche eines Erwachsenen von 1,70 m Körpergröße hat eine Ausdehnung von 1,7 bis 1,8 Quadratmeter und macht 20% des Gesamtkörpergewichts aus. Bei einem Gewicht von 70 kg wiegt die menschliche Haut 14 kg (10 kg Unterhaut, 4 kg Deckhaut). Die Deckhaut im Gesicht ist etwa 1 mm und am Gesäß 3 mm dick. Die Haut speichert 1/4 des im Körper enthaltenen Wassers (ca. 72% des Hautgewichts).
Bei der obersten Hautschicht, der Epidermis, bilden Fette (Talg) zwischen den Zellen zusammen mit den Hornzellen eine wasserabweisende Schutzschicht. Diese 10 bis 20 µm dicke Horn(zell)schicht, das Stratum corneum, ist aber keine völlig impermeable Barriere für exogene Stoffe. Die Permeationsbarriere lässt im geringen Maße Wasserdampf, Sauerstoff oder andere Gase durch [15]. An Handflächen und Fußsohlen ist das Stratum corneum am dicksten; Hydrocortison wird als Modellsubstanz vermindert resorbiert. Arzneistoffe lassen sich über unterschiedliche Wege transdermal in den Organismus aufnehmen. Die Resorptionsrate durch die Haut der Hinterohrregion und das Skrotum ist bis zu 40-fach erhöht im Vergleich zum Unterarm. Für eine Diffusion der Arzneistoffe in tiefere Hautschichten bieten sich Haarfollikel, Talg- und Schweißdrüsen an. Diese Strukturen machen aber nur etwa 0,1% der gesamten Hautoberfläche aus und dürften somit quantitativ keinen großen Effekt haben [7]. Ausschlaggebend sind Applikationsort und Hautdicke für eine dermale Arzneistoffliberation. Aus dem 1. Fick’schen Diffusionsgesetz kann der Wirkstofffluss durch das Stratum corneum abgeleitet werden. Der Vorgang der Diffusion kommt zustande, wenn zwischen zwei aneinander grenzenden Bereichen ein Konzentrationsunterschied besteht; so kommt es zu einem passiven Stofftransport aus dem einen (höher konzentrierten) in den anderen (verdünnteren) Bereich.

Aus der thermodynamischen Aktivität des Arzneistoffs ergeben sich die Einflussfaktoren auf die Wirkstoffkonzentration als treibender Faktor. In Abhängigkeit davon, ob der Stoff gelöst oder kristallin suspendiert vorliegt, ergeben sich besondere Risiken und Chancen. Die kristalline Phase eines Stoffs erzeugt aufgrund eines schnelleren Nachlösens eines Wirkstoffs eine hohe und gleichmäßige thermodynamische Aktivität. Im gelösten Zustand nimmt dieser Antrieb während der Freisetzung mit der Zeit ab. Somit nimmt auch der Wirkstofffluss ab [15]. Eine Wirkstoffübersättigung der TTS-Matrices ist das Resultat eines bewussten Entwicklungsprozesses.
Substanzen mit unterschiedlichen chemischen Strukturen kommen als Enhancer infrage, um die Diffusion von Arzneistoffen durch das Stratum corneum voranzutreiben. Als Trägerstoffe oder Permeationspromotoren kommen neben Ölsäure Harnstoff, Adipinsäurederivate und Propylenglycol zum Einsatz; bei bestimmten Wirkstoffen wird Ethanol zugesetzt. Dabei ist der Mechanismus der Permeationsbeschleunigung ungeklärt. Die Arzneistoffabgabe bei Estradiol hängt linear von der vorgegebenen Ethanolpermeation ab. Bei Testosteron-TTS kann die Verarmung an Ethanol als Enhancer dazu genutzt werden, die Wirkstofffreisetzung so zu regulieren, um zirkadiane Plasmaspiegel mit einem Maximum in den frühen Morgenstunden zu erzielen, wenn das Pflaster gegen 22 Uhr aufgeklebt wurde [7].
Die Hautklebrigkeit ist ein Kennzeichen der TTS und bietet Therapievorteile wie leichte Zugänglichkeit der Applikationsstelle, sofortige Entfernbarkeit und Beobachtungsmöglichkeit. Gleichzeitig ist die Klebeeigenschaft ein Qualitätsmerkmal. Es müssen Adhäsion, Fließfähigkeit und Kohäsion abgestimmt werden. Der Kleber muss Bewegungen und individuellen mikroskopischen Strukturen folgen.
Polyethylen, festes Kerzenwachs und Gummi sind kohäsiv, dreidimensional fixiert (durch Kristallisation oder Quervernetzungen), sie fließen nicht und sind nicht klebrig. Die Gegenspieler Kohäsion und Fließfähigkeit müssen optimiert werden [15].

Durch Wechselwirkungen mit dem Stratum corneum ändert sich die Eigenschaft der Verklebung, wobei Lipide und niedermolekulare Stoffe in den Klebefilm diffundieren. Wird das TTS nach Stunden oder Tagen abgezogen, wirkt die Klebeschicht nicht mehr klebrig, da die obere Stratum-corneum-Schicht Teil des Verbunds geworden ist. Somit beeinflussen bei längerem Tragen individuelle Hauteigenschaften die Klebrigkeit mehr als die Formulierung selbst. Sie ist auch nicht so fließfähig, dass sie durch zu weiche Polymere zu „kaltem Fluss“ führt [15], wenn sie gut formuliert sind; das Gleichgewicht zwischen Klebeverhalten und kaltem Fluss ist nicht immer optimal einstellbar. Sie sollten keine Ränder vom Tragen hinterlassen.
Druckempfindliche Haftkleber („pressure sensitive adhesives“ = PSA) sind hochviskose, elastische Stoffe, die nach kurzem, leichtem Anpressdruck sofort und dauerhaft auf der Haut kleben. Dabei müssen die Substanzen generell sowohl starke Kohäsions- als auch Adhäsionskräfte aufweisen. Haftkleber sollten, wegen des Fettfilms auf der Haut, einen eher lipophilen Charakter aufweisen. Aufgrund ihrer Viskoelastizität passen sie sich sehr gut auf die Haut verschiedener Körperzonen an und eignen sich deshalb für eine Vielfalt von medizinischen Anwendungszwecken. Zudem lassen sie sich zumeist zu einem späteren Zeitpunkt wieder vom Substrat ablösen, ohne dieses dadurch zu zerstören. Es werden Polyacrylate verwendet, die gute Druckklebeeigenschaften, einen hypoallergenen Charakter und eine gute Permeabilität für Wirkstoffe besitzen. Zudem wird Polyisobutylen in einer Mischung aus hochmolekularen Polymerketten mit Molekülen kürzerer Kettenlänge oder mit Paraffin genutzt. Die dritte Substanzgruppe sind die Silikone, die Kondensationsprodukte von Polydimethylsiloxan („Polymer“-Komponente) mit einer dreidimensionalen Silikat-Struktur („Harz“-Komponente) darstellen. Die etwas geringere Klebeeigenschaft der Silikone wird durch die Möglichkeit des häufigeren Anklebens ausgeglichen. Möglich machen das Silikonpolymere, die einen verminderten „Stripping“-Effekt (Abziehen der obersten Epidermisschicht) zeigen. Der Zusatz von Harzen, wie z.B. Kolophoniumderivate, erhöht die bioadhäsive Haftung durch Erniedrigung der Viskosität und Erhöhung der Benetzungseigenschaften der Haut. Nachteil ist ein etwas gesteigertes Potenzial zu mangelnder Hautverträglichkeit bei Haftklebern, basierend auf synthetischen Kautschukpolymeren und klebrigmachenden Harzen. Hautreizungen treten hingegen bei Polyacrylat- oder Silikonhaftklebern weitestgehend nicht auf. Eine gleichmäßige hohe Klebekraft bei allen Patienten ist ein wichtiges, aber noch nicht erreichtes Ziel.

Die Verpackung sollte von Hand (die Klebefläche nicht mit den Fingern berühren) geöffnet werden. Um das Pflaster zu schützen, sollte es nicht zerschnitten werden, da sonst das Risiko des Auslaufens des Wirkstoffs besteht. Membrankontrollierte TTS keinesfalls zerschneiden; das Zerschneiden der TTS-Matrix-Pflaster sollte von geschultem Personal durchgeführt werden, da Fehldosierungen auftreten können. Wenn sich das Pflaster vor Ablauf der Anwendungsdauer löst, sollte zuerst versucht werden, es erneut aufzukleben. Ist dies nicht möglich, kann das Pflaster mit einem medizinischen Klebeband befestigt werden, oder es kann ein neues TTS verwendet werden. Niemals sollte ein okklusives Pflaster wie Tegaderm™ über das TTS geklebt werden, da es die Absorption verändern kann (Ausnahme: Emla® Pflaster).
Vor einer MRT-Untersuchung müssen alle TTS entfernt werden, da TTS z.T. neben Kunststofffolien über ein Metallgerüst (Aluminium) verfügen, das elektrischen Strom leiten kann. Die enorme Hitzeentwicklung kann zu Gewebeschädigungen und Verbrennungen zweiten Grades führen. Nur TTS mit einer aluminisierten Rückschicht müssen entfernt werden; transparente TTS sind in der Regel aluminiumfrei. Im Zweifelsfall sollte den Angaben der Fachinformation Folge geleistet werden.
Zudem kann durch Hitzeeinwirkung auf das TTS die Absorptionsgeschwindigkeit zunehmen, weshalb Wärme (Heizdecken, Wärmflaschen oder Sonnenlicht) auf die TTS nicht angewendet werden darf. Die Absorptionsgeschwindigkeit und damit die Plasmakonzentration erhöhen sich signifikant durch die verbesserte Durchblutung der Haut und zerstören die Arzneistoffreservoirs. Eine trockene Lagerung bei Raumtemperatur in der Originalverpackung ist sinnvoll. Sinnvoll ist es auch, die ersten zwei Wochen weniger intensiven Sport zu betreiben, Sport in extremer Hitze und Feuchtigkeit zu meiden, kühlere Tageszeiten zu bevorzugen, lockere und luftdurchlässige Kleidung zu tragen und den Patienten aufzuklären. TTS müssen auf gesunde, nicht gereizte, trockene (Seifen, Öle, Lotionen und hautreizende Substanzen meiden), flache, saubere, nicht behaarte, möglichst faltenfreie, nicht irritierte oder bestrahlte Hautstellen angeklebt und 30 Sekunden angepresst werden. An der Applikationsstelle sollten die Haare mit einer Schere entfernt, aber nicht rasiert (Hautreizung) werden. Applikationsorte ständig wechseln. Die Applikationsstellen für die einzelnen TTS sind der Packungsbeilage zu entnehmen. Ratsam ist eine Klebestelle, die sich bei Körperbewegungen nicht stark faltet. Nach Aufkleben von Scopoderm®-TTS Hände waschen. Estradiolpflaster nicht auf die Brust kleben. Schmerzpflaster müssen nicht auf die schmerzende Stelle geklebt werden. Vorzeitig von der Haut gelöste Pflaster müssen durch neue ersetzt werden (Patienten frühzeitig auf Vorrat hinweisen). Benutzte TTS zusammenfalten und im Hausmüll, für Kinder unzugänglich, entsorgen [7] [15] [16].
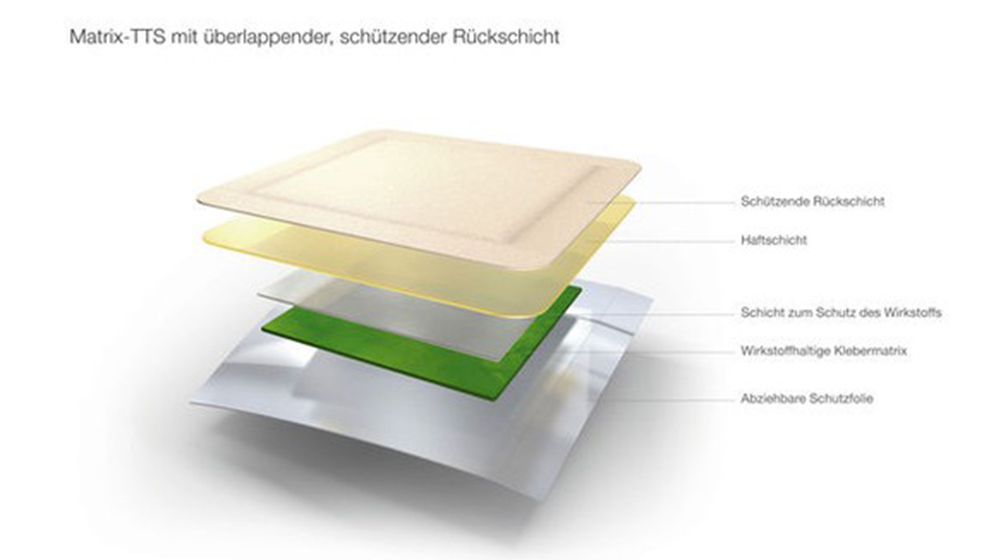
Aus historischer Sicht werden die TTS in zwei große Klassen der kontrollierten Wirkstoffabgabe klassifiziert: Membran- und Matrixpflaster.
Das Membranpflaster ist gekennzeichnet durch eine relativ konstante Liberation. Auf membrankontrollierten Systemen basieren alle Entwicklungen der TTS. Sie haben eine Polymermembran, die die Permeation eines Arzneistoffs aus einem Reservoir in die Haut kontrolliert. Eine potenzielle Gefahr: Bei mechanischer Verletzung der Kontrollmembran kann das (flüssige) Wirkstoffreservoir aus dem Depot schlagartig freigesetzt werden (engl.: „dose-dumping“). In Matrixpflastern liegt der Wirkstoff gebunden vor; sie weisen dieses Risiko nicht auf.
Die klassischen Membransysteme besitzen eine Reservoirschicht, die an eine Abdeckschicht angrenzt, in der der Wirkstoff in kristalliner oder gelöster Form vorliegt. Auf der nächsten Schicht, der Kontrollmembran, ist eine polymere Klebeschicht aufgebracht, die den Hautkontakt ermöglicht. Dabei stellt die Kontrollmembran eine Permeationsbarriere im Diffusionsverlauf dar [15]. Die Klebeschicht und die Haut erreichen weniger thermodynamische Aktivität, je restriktiver die Membran ausgelegt ist. Somit ist der Streuanteil der Haut geringer.
Unter der Trägerfolie befindet sich ein Wirkstoffreservoir, aus dem kontrolliert durch eine poröse Membran die Arznei abgegeben wird. Bei beiden Techniken diffundiert (passiver Vorgang) die Arznei durch die Haut und gelangt durch die Blutgefäße in den Blutkreislauf. Der Arzneistoff passiert nur in niedrigen Mengen durch Poren und Haarfollikel in die Haut. Er wird häufig durch mikroskopisch kleine Zellzwischenräume oder durch die Zelle selbst resorbiert/aufgenommen. Voraussetzung ist seine Fettlöslichkeit (Lipophilie).
Für eine transdermale Applikation kommen generell nur Wirkstoffe infrage, die eine relativ kleine Molekülgröße besitzen und zudem schon in geringen Dosierungen wirksam, also hochpotent sind.
Bei Matrixsystemen ist der Aufbau simpler, da sie kein separates Kontrollelement besitzen. Eine lipophile oder hydrophile Polymermatrix kontrolliert die Arzneistoffabgabe. Dort liegt der Wirkstoff gelöst oder homogen dispergiert vor. Matrixdiffusionskontrollierte Systeme setzen die Wirkstoffe nicht immer zeitkonstant frei. Weil „dose-dumping“ nicht möglich ist, ist diese Arzneigabe bei hochaktiven Arzneistoffen ungefährlich [7], wobei jede Verabreichung von Arzneien gefährlich sein kann, aber das besondere Risiko der unbeabsichtigten Überdosierung durch „dose-dumping“ ist hier nicht präsent.

Weiterentwicklungen steuern die Arzneistoffliberation zeitkonstant. Moderne Matrixsysteme besitzen neben der Abdeckschicht nur noch eine Schicht. Diese übt gleichzeitig die drei Funktionen des Wirkstoffreservoirs, des Kontrollelements und der Haftschicht („drug-in-adhesive“) aus. In sogenannten Multilayersystemen ist der Wirkstoff von oben nach unten in abnehmender Konzentration verteilt. So wird nach Applikation ein beständiges Konzentrationsgefälle als treibendes Element für eine zeitkonstante Arzneistoffliberation aufgebaut [7]. Damit wird eine potenziell nachlassende Wirksamkeit verhindert. Die Multilayersysteme wirken bei opiatnaiven Anwendern einer Atemdepression entgegen. Weil sich im subkutanen Fettgewebe ein Depot aufbaut, wirkt der Wirkstoff nach Entfernen des Pflasters noch nach. In der Matrix befindet sich der Wirkstoff in einer oder mehreren Schichten vor. Sie liegt mittels Klebeschicht direkt auf der Haut auf. Die Resorptions- geschwindigkeit wird durch die Diffusionsgeschwindigkeit des Wirkstoffs aus der Matrix definiert. Die Wirkstoffabgabe kann durch eine zusätzliche Membran zwischen Matrix und Klebeschicht gelenkt werden. Bei der Variante der Matrix mit „Innerer Phase“ verwendet man verträgliche physiologische Lösungsmittel mit gewisser Eigenresorption. Damit lassen sich die Rekristallisationen vermeiden, die während der Lagerung entstehen. Beim Tragen ermöglichen sie den Nutzen von zeitweise durch Entzug des Lösungsmittels auftretenden Übersättigungserscheinungen. Es werden auch feste, polymere, wasserquellende Strukturen in die Schichten eingebettet. Sie binden die Hautfeuchtigkeit und unterstützen die Klebekraft. Aber es können auch schwer lösliche Wirkstoffe als „feste Lösungen“ eingesetzt werden. Durch die Hautfeuchtigkeit werden wirkstoffhaltige Polymerpartikel wieder Teil der Diffusion. Bei Sättigung des Systems mit Wasser und der dadurch reduzierten Löslichkeit kann es zu einer Wirkstoffübersättigung kommen. Inkompatible Polymere schaffen Kompromisse, wobei sich submikroskopische Phasengrenzen ergeben (PVP-Silikonpolymere; Acrylate-Silikonpolymere) [15]. Das macht die Wirkstoffgabe unkomplizierter, besser und preiswerter. Dazu ergeben sich auch ganz neue Perspektiven, an denen die Forscher arbeiten, um die Hautpflaster noch aktiver und intelligenter zu machen.
Aktuelle Medikamentenpflaster haben keine Gemeinsamkeiten mehr mit den Vorgängermodellen, bei denen die wesentlichen Arzneistoffe wie in einen Teebeutel verpackt auf die Haut geklebt wurden. Heute können High-Tech-Kunststoffe die Substanzen fein dosiert abgeben. Aber nicht alle Wirkstoffmoleküle bewegen sich von allein und ohne technische Hilfe durch die Haut. Aktuelles Ziel ist es, sehr große Moleküle, etwa Antikörper gegen Krebs oder Impfstoffe, mithilfe von kleinen Strom- oder Laserimpulsen durch die Haut zu applizieren. Diese aktiven transdermalen Systeme müssen dann auch eine dünne Batterie mit sich tragen.
Die aktiven transdermalen Systeme sind eine Weiterentwicklung. Sie nutzen iontophoretische oder sonophoretische Methoden sowie Systeme mit Mikrokanülen oder Nadeln. Die Nadeln durchdringen die oberen Hautschichten und gelangen unmittelbar an ihren Bestimmungsort.

Die mechanische, elektrische oder chemisch-physikalische Vorbehandlung der Haut reduziert ihre Barrierefunktion. Durch Ultraschall oder gleichzeitiges Anlegen elektrischer Spannung ergeben sich andere Wege, um die Möglichkeit von transdermalen therapeutischen Systemen zu nutzen. Der Einsatz von aktiven Systemen, etwa unter Nutzung von Iontophorese, Elektroporation, Ultraschall oder Mikronadeln, beeinflusst die Hautbarriere und verstärkt die Permeation. Die nichtinvasive Iontophorese nutzt ein sehr geringes elektrisches Feld, das schwachen Gleichstrom durch die Haut leitet, um geladene Moleküle zu transportieren. Ein Iontophorese-TTS vereinigt einen Mikroprozessor und eine Batterie, zwei Elektroden und die Pflasterkomponenten. Die Elektroden sind beide reine elektronische Bauteile; unter den Elektroden befinden sich ein wirkstoffhaltiges und ein wirkstofffreies Kompartiment. Damit lässt sich die Wirkstoffabgaberate über den elektrischen Strom kontrollieren, der wiederum durch den Mikroprozessor präzise gesteuert wird. Das iontophoretisch (oder iontopheretisch) arbeitende TTS bietet eine nichtinvasive Technik durch Anlegen eines schwachen elektrischen Feldes, das den Wirkstoff durch die Haut schleust. Die Arzneistoffe müssen als Ion (ionisiert) vorliegen, also eine eigene elektrische Ladung haben. Das ist Voraussetzung, um sie im elektrischen Feld zu beschleunigen und somit die Permeationsrate zu erhöhen.
Solche Systeme erreichen eine Stromstärke von etwa 10–30 mA. Wie beim Stangerbad (Hydroelektrisches Vollbad bzw. Hydroelektrisches Dreiviertelbad) kann von 0 allmählich auf den Endwert hochgeregelt und bei Ende der Behandlung ebenso heruntergeregelt werden. Die für den Stromfluss benötigte maximale Spannung liegt dann bei etwa 60 Volt. Der Patient kann durch Knopfdruck eine Dosis von 40 Mikrogramm freisetzen.
Auf dem Markt sind Systeme mit Fentanyl und Lidocain, die nicht größer als eine Kreditkarte sind. Wie der Wirkstoff dosiert wird, kann wie bei dem Einmalpflaster durch Knopfdruck vom Patienten bestimmt werden.
Mittels Iontophorese können Substanzen transdermal verfügbar gemacht werden, die aufgrund ihrer Eigenschaften nicht für passive Systeme geeignet sind, wie z.B. geladene Moleküle.
Die partielle Perforation des Stratum corneum und die anschießende Applikation eines TTS lassen die Permeationsrate signifikant steigen. Dazu nutzt man eine weitestgehend schmerzfreie Perforation der obersten Hautschicht mit Mikronadeln, die gerade lang genug sind, damit die äußerste Hautschicht durchdrungen werden kann. Sie sind aber zu kurz, um Nerven und Blutgefäße zu reizen. Die einzelnen Mikronadeln sind winzig klein: < 1 mm, in der Regel zwischen 300 und 800 µm. Mikronadeln erzeugen kleine Löcher, um Substanzen durch die Haut zu schleusen. Damit wird die Wirkstoffaufnahmerate signifikant erhöht.
US-amerikanische Forscher haben ein Impfpflaster entwickelt, das die Vakzine gegen Influenzaviren in Zukunft vereinfacht. Auf seiner Oberfläche besitzt das Pflaster hunderte Mikronadeln aus Polyvinylpyrrolidon. Die Mikronadeln, in die der Impfstoff eingeschlossen ist, dringen etwa 0,65 mm tief in die Epidermis ein. Sie lösen sich dort innerhalb von Minuten nach Applikation auf, wobei der Impfstoff freigesetzt wird. Dieser erreicht dann die Antigen präsentierenden Zellen (engl.: antigen-presenting cells, kurz: APC), also Fresszellen, der Haut.
Die Wirkung des Impfpflasters wurde an Mäusen getestet. Die positive Immunantwort schützte die Mäuse gegen die sonst tödlichen Grippevirusgaben. Das Impfpflaster war sogar geringfügig effektiver im Vergleich zur üblichen intramuskulären Impfung. Das Pflaster mit Mikronadeln könnte zukünftig statt der Impfung per Spritze bei verschiedenen Krankheitserregern verwendet werden. Das würde zudem die Logistik vereinfachen. Auch Menschen ohne medizinische Kenntnisse könnten die Pflaster verabreichen. So lassen sich während einer Pandemie Personalengpässe vermeiden. Das System ließe sich theoretisch auch gegen andere Krankheitserreger anwenden. Vor dem Markteintritt müssen klinische Studien beweisen, dass das Präparat sicher und wirksam ist [8].
Der Wirkstoff Sumatriptan kann Anfälle von Schmerzen und Übelkeit durch aktive Applikation eines Triptans unterdrücken und vermeiden. In den USA wurde das Einmalpflaster (Sumatriptan iontophoretisches transdermales System) für die Migränetherapie von der FDA 2013 zugelassen. Auf Arm oder Oberschenkel geklebt, gibt das Pflaster, nach einer Aktivierung per Knopfdruck, über vier Stunden durch Iontophorese 6,5 mg Sumatriptan ab. Ein Mikroprozessor im Pflaster misst währenddessen kontinuierlich den Hautwiderstand und reguliert die Abgabe des Arzneimittels.
Indiziert ist es für die Behandlung von Erwachsenen, die unter akuter Migräne mit oder ohne Aura leiden. Der Zulassung liegen Daten aus drei klinischen Studien mit 800 Patienten und über 10.000 Anwendungen zugrunde. 53% der mit dem Einmalpflaster behandelten Patienten erreichten eine Linderung der Kopfschmerzen und 84% waren binnen zwei Stunden von Übelkeit befreit; unter Gabe von Placebo waren es 29% und 63%. Innerhalb von zwei Stunden waren 19% der Patienten komplett von ihren Kopfschmerzen befreit; unter der Gabe von Placebo 9%. Bei 2% der Patienten wurden triptanassoziierte unerwünschte Wirkungen beobachtet. Häufigste Nebenwirkungen waren Kribbeln und Wärmegefühl am Applikationsort sowie Unwohlsein. Profitieren sollen besonders Patienten mit migräneassoziierter Übelkeit oder Gastroparese. Denn Erbrechen oder verlangsamte gastrointestinale Resorption kann die Wirkung oraler Arzneimittel verringern [13].
Innovativ ist auch das Empfangen und Speichern von Signalen, um Auskunft über den Wirkstoffgehalt im Körper zu bekommen. Deswegen vermarktet der chinesische Lenovo Konzern gemeinsam mit Novartis und anderen Unternehmen unter dem Namen „Proteus Digital Health Pill“ solch einen Datenempfänger (MC10) in Pflasterform bzw. als Elektro-Tattoo: Die Patienten schlucken nur noch einen sandkorngroßen Minisensor, der den Wirkstoffspiegel im Körper misst und die Ergebnisse dem Pflaster meldet. Die eine Seite ist mit Magnesium und die andere Seite ist mit Kupfer beschichtet. Trifft der Sensor auf Magensäure, erzeugt er dank kleiner Spannung ein elektrisches Signal. Das 18-Bit-Signal wird von einem speziellen Pflaster empfangen und z.B. an das Mobiltelefon weitergegeben. So kann der Arzt die Medikamenteneinstellung kontrollieren. Sollte der Patient die Einnahme vergessen, sendet das Digitalpflaster eine Erinnerung aufs Handy.
Schweizerische Forscher der Eidgenössischen Materialprüfungs- und Forschungsanstalt (EMPA) entwickelten ein TTS, das Wirkstoffe kontinuierlich über eine Membran abgibt, wenn diese mit UV-Licht bestrahlt wird. Die Membran hält ohne Bestrahlung mit Weißlicht Wirkstoffe im Depot zurück. Die Medikamente diffundieren durch eine lichtempfindliche Membran über die Haut in den Körper, wobei die Abgaberate der Medikamente steuerbar ist. Die Membran wird mittels Spiropyranen durchlässiger, wenn sie mit UV-Licht beleuchtet wird. Die Abgaberate wird über die Bestrahlung der Membran durch unterschiedliche Lichtfarben geregelt.
Die so im Wasser entstandenen gelösten Moleküle (Hydrophile), also polare Verbindungen, diffundieren dann einfacher durch das Pad. Fällt weißes Licht auf die Membran, werden die Spiropyrane wieder deaktiviert und zurück in ihren anfänglichen, wasserabweisenden Zustand versetzt. Arzneimittel, die dann im Wasser gelöst sind, diffundieren kaum oder gar nicht mehr durch die Membran. Dieser Prozess lässt sich dann über mehrere Stunden regulieren. Das Projekt fokussiert sich hauptsächlich auf die Koffeingabe bei Neugeborenen, um Atemstillstände zu vermeiden. Es ist nicht auszuschließen, dass die Membran sich auch für andere Arzneistoffe, wie Theophyllin oder Lidocain, verwenden lässt [9].
Literatur
1. www.wiwo.de/technologie/forschung/medikamente-impfstoffe-und-co-was-das-pflaster-der-zukunft-alles-kann/7427520.html
2. www.md-institute.com/cms/wundversorgung.html
3. www.subletter.de/sites/default/files/subletter_06-2012-ohne-Werbung_0.pdf
5. www.awmf.org/uploads/tx_szleitlinien/091 001l_S3_Lokaltherapie_chronischer_Wunden_2012-06.pdf
6. www.kvno.de/downloads/newsletter/vin/VIN_04_2013_2.pdf
7. www.pharmazeutische-zeitung.de/index.php?id=24037
8. Dissolving Polymer Microneedle Patches for Influenza Vaccination. Nature Medicine 16, 915–920 doi:10.1038/nm.2182. Received Accepted Published online. Dissolving Polymer Microneedle Patches for Influenza Vaccination. Sean P. Sullivan, Dimitrios G. Koutsonanos, Maria del Pilar Martin, Jeong Woo Lee, Vladimir Zarnitsyn, Niren Murthy, Richard W. Compans, Ioanna Skountzou, Mark R. Prausnitz. www.ncbi.nlm.nih.gov/pmc/articles/PMC2917494/
9. www.empa.ch/plugin/template/empa/*/152072/---/l=1
10. www.medica.de/cipp/md_medica/custom/pub/content,oid,50684/lang,1/ticket,g_u_e_s_t/~/Medikamente_mit_Wirkstoffmembran_schonend_applizieren.html
11. www.ema.europa.eu/docs/en_GB/document_library/Scientific_guideline/2014/12/WC500179071.pdf
12. www.novartispharma.com/newsroom/media-releases/en/2013/1716888.shtml
13. www.marketwired.com/press-release/nupathes-zecuity-approved-by-the-fda-for-the-acute-treatment-of-migraine-nasdaq-path-1747184.htm
14. granulox.de/wpcontent/uploads/2012/10/Granulox_Heilberufe_2012_Dossier_1.pdf
15. Innovative Arzeiformen: Ein Lehrbuch für Studium und Praxis, Karsten Mäder (Herausgeber), Uwe Weidenauer (Herausgeber), Daniela Allhenn (Assistent) & 28 mehr, Wissenschaftliche Verlagsgesellschaft; Auflage: 1 (1. Oktober 2009), Seite 302–321
16. Sports Medicine, Volume 41, Issue 3, pp 177–183; Transdermal Patch Drug Delivery Interactions with Exercise; Thomas L.Lenz, Nicole Gillespie
17. http://archneur.jamanetwork.com/article.aspx?articleid=1704351
Entnommen aus MTA Dialog 4/2016
Dann nutzen Sie jetzt unser Probe-Abonnement mit 3 Ausgaben zum Kennenlernpreis von € 19,90.
Jetzt Abonnent werden

