Einen Monat später erreichte die erste Welle mit über 6.000 registrierten Neuinfektionen pro Tag auch hierzulande ihren Scheitelpunkt, doch niemand konnte damals gesicherte Aussagen über die Dunkelziffer machen. Der Grund: Die PCR-Testkapazitäten reichten nicht einmal aus, alle symptomatischen Patienten zu testen, Antigen-Schnelltests waren noch nicht verfügbar und zur Aussagekraft von Antikörpertests lagen keine belastbaren Studien vor. Für mich persönlich bleiben aus dieser Zeit vor allem die Hilferufe in Erinnerung, die unseren Verlag aus den Laboren erreichten. Die Politik forderte zwar unter dem Slogan „testen, testen, testen“ eine dramatische Erhöhung der Analysenzahlen, doch es blieb lange Zeit unklar, was man wie testen sollte, fehlte es doch zu Beginn der Pandemie an allem: Für die PCR gab es nur Forschungsreagenzien und ein vorläufiges Testprotokoll der Charité, Geräte für die Nukleinsäureextraktion wurden zu Schwarzmarktpreisen gehandelt und nicht einmal für die Abstriche reichten die Tupfer aus.
Unsere Leser erhofften sich rasche Antworten auf scheinbar einfache Fragen wie zum Beispiel:
- Kann man Q-Tipps verwenden, wenn keine Abstrichbestecke verfügbar sind?
- Würden Sie eine PCR notfalls auch ohne Nukleinsäureextraktion durchführen?
- Darf man Assays einsetzen, die nicht CE-/IVD-zertifiziert sind?
Für diesen brisanten Informationsbedarf waren die Reaktionszeiten einer Quartalszeitschrift wie Trillium Diagnostik viel zu lang. Deshalb trommelten wir innerhalb weniger Tage ein Expertenteam aus Virologen, Immunologen und Labormedizinern zusammen und verschickten die Antworten per Newsletter: Q-Tipps: ja; PCR ohne RNA-Extraktion: nein; Assays ohne Zertifikat: „im Prinzip ja, aber … “. Der Bedarf an Expertise ist auch heute, eineinhalb Jahre nach Beginn der Pandemie, ungebrochen, doch die Fragen haben sich gewandelt (Abb. 1). Ging es anfangs vor allem um technische Probleme, so stehen inzwischen Variantentestung, Impfantwort und COVID-19-Langzeitfolgen im Vordergrund.
Teststrategien für den Virus- und Antikörpernachweis
Die offizielle Grundlage für die Auswahl von Tests zum direkten Erregernachweis ist die sogenannte „Nationale Teststrategie SARS-CoV-2“, die das Gesundheitsministerium im Internet bereitstellt [1]. Dort ist insbesondere geregelt, dass eine PCR-Testung bei allen symptomatischen Patienten bei bekannter Exposition, bei Ausbrüchen sowie in vulnerablen Bereichen wie etwa Krankenhäusern und Arztpraxen vorgeschrieben ist. Antigentests werden dagegen für Reihenuntersuchungen (Screening) in Betrieben oder Schulen sowie für sogenannte Bürgertests und Eigenkontrollen empfohlen.
Diese Strategie stammt allerdings vom März 2021 und wurde seither nicht mehr aktualisiert. Sie berücksichtigt insbesondere zwei neuere Entwicklungen nicht:
- PCR-Pooltestungen anstelle von Antigentests
- Antikörpertests zur Kontrolle der Impfantwort
Bei der Pooltestung geben bis zu 30 Personen (zum Beispiel eine Schulklasse) Gurgelwasser ab, das mit einer hochempfindlichen PCR analysiert wird. Fällt das Poolergebnis positiv aus, werden die individuellen Rückstellproben nachgetestet. In einer Pilotstudie zeigte sich, dass dieses Verfahren nicht nur einfacher und kostengünstiger, sondern auch empfindlicher und sicherer ist als die derzeit massenhaft an Schulen durchgeführten Schnelltests – von der Vermeidung gewaltiger Berge an Plastikmüll ganz abgesehen.
Antikörpertests spielen in der Nationalen Teststrategie Deutschlands noch keine Rolle, obwohl andere Länder wie etwa Österreich, Italien oder Frankreich damit das Pandemie- und Impfgeschehen bereits erfolgreich überwachen. Im Kontext der Impfung sind zwei Indikationen wichtig:
1. Die Höhe der Titer gegen das virale Spike-Protein (Anti-S) gibt Auskunft über die Qualität der Impfantwort. Mit einer verminderten Reaktion ist bei alten Menschen, Krebspatienten oder Immunsupprimierten zu rechnen; besonders hohe Titer werden nach „Kreuzimpfung“ mit einem Vektor- und einem mRNA-basierten Vakzin beobachtet.
2. Antikörper gegen das virale Nukleokapsid-Protein (Anti-N) lassen dagegen erkennen, ob bereits eine (möglicherweise asymptomatische) Infektion vorliegt. In diesem Fall sollte erst nach einem halben Jahr geimpft werden, um eine überschießende Immunreaktion mit heftigen Nebenwirkungen zu vermeiden, und eine Zweitimpfung ist entbehrlich.
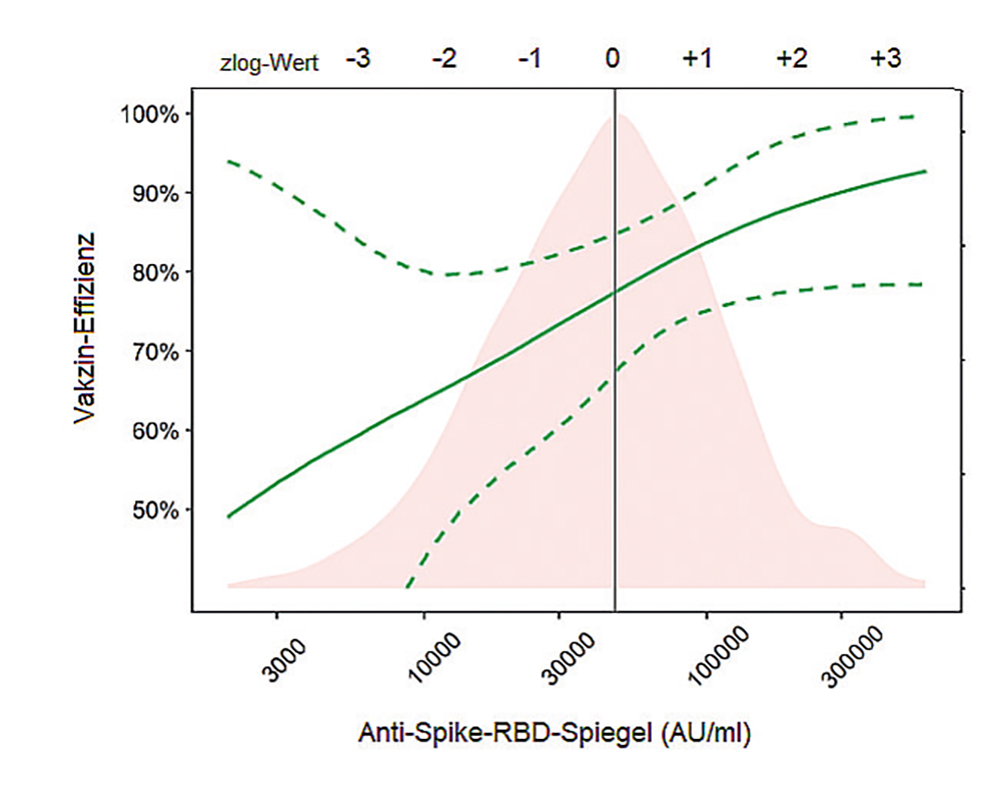
Abb. 2: Die Anti-Spike-RBD-Spiegel nach Impfung folgen einer Lognormalverteilung (rosa Kurve), die als Grundlage der Standardisierung mit dem zlog-Verfahren dienen könnte. Die y-Achse zeigt, dass die Schutzwirkung bei einem zlog-Wert von –3 (entsprechend etwa 4.000 AU/ml) mit etwa 50 % gering und bei einem Wert von +3 (> 300.000 AU/ml) nahezu 100 % wäre. Abbildung modifiziert nach Ref. 3.
Nach einer Erhebung des VDGH e.V. besteht in der Bevölkerung ein großes Interesse an solchen Antikörperbestimmungen. Pro Woche führen niedergelassene Labore aktuell (Stand: Juni 2021) etwa 100.000 Tests durch, von denen mindestens 60 % aus eigener Tasche bezahlt werden müssen. Dass diese Tests derzeit noch nicht empfohlen werden, begründet das RKI vor allem mit der mangelnden Standardisierung der im Markt befindlichen Assays. Je nach Hersteller können die Werte zwischen 1 und 100, 10 und 1.000 oder auch weit über 1.000 liegen. Das erschwert die Interpretation und kann Laien verunsichern.
Im Rahmen eines Projekts zur elektronischen Patientenakte stellten wir 2017 einen Vorschlag zur Standardisierung von Laborwerten vor [2], der auch zur Standardisierung von Antikörperspiegeln gegen SARS-CoV-2 herangezogen werden könnte. Der sogenannte zlog-Wert drückt Laborwerte nicht absolut, sondern relativ als Abweichungen vom Referenzbereich aus: Ein zlog-Wert von 0 besagt, dass der Messwert genau im Zentrum des Referenzbereichs liegt, erhöhte Werte sind positiv, erniedrigte negativ. Abbildung 2 zeigt am Beispiel von Anti-Spike-RBD-Werten, wie dieses Verfahren sinngemäß im Monitoring der Impfantwort eingesetzt werden könnte. Anstelle des Referenzbereichs wird hier die typische Impfreaktion einer gesunden Kontrollgruppe als Referenz verwendet. Die zlog-Werte erlauben dann völlig unabhängig von der absoluten Höhe der Spiegel eine Einordnung, ob die Antwort des Immunsystems ausreichend oder schwach ausgeprägt ist. Das Verfahren wird derzeit klinisch evaluiert.
Wer sich für die statistischen Grundlagen der Labordatenstandardisierung und Referenzintervallermittlung interessiert, sei an dieser Stelle auf die zertifizierten E-Learning-Kurse der Trillium Akademie hingewiesen (www.trillium.de).
Kontakt: georg.hoffmann@trillium.de
Literatur
1. www.bundesgesundheitsministerium.de/fileadmin/Dateien/3_Downloads/C/Coronavirus/Nationale_Teststrategie_kurz.pdf.
2. Hoffmann G, et al.: Der zlog-Wert als Basis für die Standardisierung von Laborwerten. J Lab Med 2017; DOI 10.1515/labmed-2016–0087.
3. Feng S, et al.: Correlates of protection against symptomatic and asymptomatic SARS-CoV-2 infection. Preprint medRxiv 2021; DOI 10.1101/2021.06.21.21258528.
Entnommen aus MTA Dialog 8/2021
Artikel teilen


