Mikropartikel – kleine Helden in der Leberregeneration
Am Translationszentrum für Regenerative Medizin in Leipzig (TRM) beschäftigt sich die Arbeitsgruppe um Dr. Moritz Schmelzle mit CD133-positiven hämatopoetischen Stammzellen (HSC) in der Leberregeneration.
Vorangegangene Untersuchungen belegen, dass HSCs Mikropartikel freisetzen, von denen angenommen wird, dass sie zur Steigerung der Leberregeneration beitragen, indem sie der Entzündungsreaktion entgegenwirken. Ausschlaggebend hierfür ist die Ektonukleotidase CD39, die extrazelluläres pro-inflammatorisches ATP in anti-inflammatorisches Adenosin hydrolysiert. In einem CD39-abhängigen Mechanismus wird unter anderem eine anti-inflammatorische mikroRNA (miR, miRNA) verpackt, welche durch andere Arbeitsgruppen bereits als immunmodulatorisch beschrieben wurde. Extrazelluläres ATP sorgt dabei für ein erniedrigtes miRNA-Level, während Adenosin die Anreicherung der MP mit dieser anti-inflammatorischen mikroRNA fördert. Weitere Ergebnisse lassen eine Funktion dieser miRNA in der Regulierung von pro-inflammatorischen Zytokinen vermuten und unterstützen die Rolle der MP als zell-spezifische Transporter in der interzellulären Kommunikation.
Mikropartikel
Unter Mikropartikeln versteht man unter 1 μm kleine Zellvesikel, bestehend aus Plasma und Zellmembran ihrer Ursprungszelle. Sie tragen in der Regel die gleichen Oberflächenmarker wie ihre Mutterzelle und können dieser somit zugeordnet werden. Mikropartikel sind im Blut nachweisbar und geben Auskunft über den jeweiligen Funktionszustand ihrer Ursprungszelle.

Abb. 1: Mikropartikel-Pellet nach Ultrazentrifugation
1967 wurden Mikropartikel erstmals von Wolf et al. als „cell dust“ beschrieben. Damals nahm man noch an, dass Mikropartikel keinerlei spezifische physiologische Funktionen besitzen. Mittlerweile konnte durch unterschiedliche Studien belegt werden, dass Mikropartikel der interzellulären Kommunikation zwischen Zellen dienen und inflammatorische Prozesse beeinflussen.
Die Isolation von Mikropartikeln aus Plasma oder Zellkulturüberständen erfolgt mittels 2-stufiger Ultrazentrifugation (1. Schritt: 10.000 g 30 min; 2. Schritt: 100.000 g 90 min). Die Analyse erfolgt anhand ihrer Oberflächenmarker im FACS (= fluorescence-activated cell sorting). Der Inhalt, insbesondere mikroRNAs, werden mittels quantitativer real-time PCR untersucht.
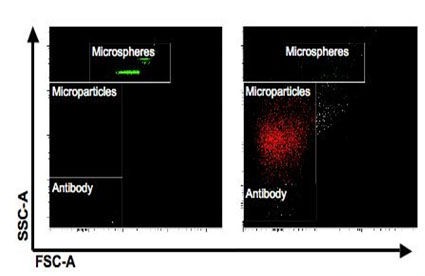
Abb. 2: FACS-Analyse
mikroRNA
Bei mikroRNAs handelt es sich um kleine, nicht kodierende RNA-Moleküle bestehend aus etwa 22 Nukleotiden. Sie sind in der Lage, mehr als die Hälfte des menschlichen Transkriptoms auf posttranskriptionellem Weg zu regulieren und spielen in vielen zellulären Vorgängen wie Zellproliferation, Apoptose und Metabolismus eine bedeutende Rolle. Unterschiede zu anderen Klassen kleiner RNA (siRNA, piRNA) liegen in der Biogenese. So wird miRNA in der Zelle auf eigenen miRNA-Genen codiert, die siRNA hingegen entsteht aus längerer freier dsRNA, die z.B. von Viren stammt.
Im Zellkern transkribiert die RNA-Ploymerase II unabhängige miRNA-Gene in primäre Transkripte, den sogenannten pri-miRNAs. Diese können einzeln oder in Clustern auftreten und sind in erster Linie dadurch gekennzeichnet, dass sie schnell sekundäre Strukturen, sogenannte hairpins, ausbilden. Der nukleäre dsRNA-bindende Proteinkomplex Drosha-DGCR8 bindet die pri-miRNA und prozessiert diese in die pre-miRNA , einer doppelsträngigen RNA von ca. 70 Nukleotiden. Die pre-miRNA wird mit Hilfe eines Transportproteins in das Zytoplasma geschleust, wo es an den Dicer-TRBP-Komplex ( TRBP = dsRNA-bindendes Protein, cytosolisch) gebunden und dort zu reifer miRNA prozessiert wird. Einer der beiden miRNA-Stränge wird im Anschluss im RISC-Komplex (RNA-induced silencing Komplex) integriert und zur Ziel-mRNA geleitet, wo es entweder zur Inhibierung der Translation oder zum Abbau der Ziel-mRNA kommt.
Purinerger Stoffwechsel in der Leberregeneration
Der purinerge Stoffwechsel beschreibt die Hydrolyse von extrazellulärem pro-inflammatorischem ATP zu anti-inflammatorischem Adenosin mittels der beiden Ektoenzyme CD39 und CD73.
Unter physiologischen Bedingungen liegt ein Gleichgewicht zwischen ATP und Adenosin vor.
Bei einer Leberschädigung verlagert sich das Gewicht zum pro-inflammatorischen ATP, welches CD39 positive hämatopoetische Stammzellen aus dem Knochenmark mobilisiert und diese aktiviert, vermehrt Mikropartikel zu bilden. Es wird angenommen, dass die Mikropartikel über die Blutbahn zur Leber gelangen und dort zusammen mit bereits anwesenden Stammzellen das überschüssige ATP zu Adenosin hydrolysieren. Die Arbeitsgruppe hat gezeigt, dass Adenosin gezielt die Verpackung der immun-assoziierten mikroRNA in die Mikropartikel vermittelt (siehe Abb. 3).
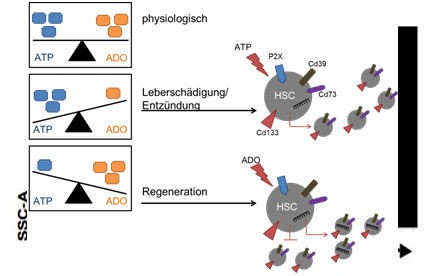
Abb. 3: Purinerger Stoffwechsel
Weiterhin zeigen erste Ergebnisse der AG Schmelzle, dass auf diese Weise angereicherte Mikropartikel in der Leber mit den Endothelzellen fusionieren und die mikroRNA in die Zielzelle abgeben können. Weiterhin konnte gezeigt werden, dass die mikroRNA die Genexpression von pro-inflammatorischen Zytokinen in den Endothelzellen reguliert sowie die Apoptoserate verringert. Pro-inflammatorische Zytokine sind als Signalstoff an lokalen Entzündungsprozessen beteiligt. Eine verminderte Genexpression führt somit zu einer verbesserten Regeneration der Leber.
Tiermodell
Die Versuchsdurchführung erfolgte in C57Bl/6 Wildtyp und Cd39 null sowie Cd73 null Mäusen nach 70 % Hepatektomie.
Mithilfe dieses Tiermodells ist es den Wissenschaftlern um Dr. Moritz Schmelzle gelungen, die bedeutende Rolle des purinergen Stoffwechsels zu untersuchen. Fehlen die beiden Ektoenzyme CD39 und CD73, ist es dem Organismus nicht mehr möglich, extrazelluläres ATP abzubauen. Dieses reichert sich an und sorgt so für einen dauerhaft entzündlichen Zustand. Eine durch die anti-inflammatorische mikroRNA vermittelte Leberregeneration, wie bereits im vorherigen Abschnitt beschrieben, bleibt aus.
Ausblick
Neben dem aktiven Mitwirken am Leberregenerationsprozess, besitzen Mikropartikel zudem ein großes Potenzial als neuartige Biomarker, um chronische Erkrankungen zu monitoren sowie den postoperativen Regenerationsprozess zu überwachen.
Die Forschungsarbeiten ermöglichen somit ein besseres Verständnis der komplexen Mechanismen der postoperativen Leberregeneration bis hin zur möglichen Applikation von Stammzell-Mikropartikeln zur Regenerationsförderung.
Die Autorin:
Cindy Hegewald
Universität Leipzig
Translationszentrum für Regenerative Medizin
AG Dr. Schmelzle
Semmelweisstraße 14
04103 Leipzig
cindy.hegewald@trm.uni-leipzig.de
Entnommen aus MTA Dialog 11/2015
Dann nutzen Sie jetzt unser Probe-Abonnement mit 3 Ausgaben zum Kennenlernpreis von € 19,90.
Jetzt Abonnent werden

